Zobacz slidy
Treść prezentacji
Slide 1
Reakcje w roztworach wodnych mgr inż. Joanna Sławna Corpora non agunt nisi soluta Ciała mogą reagować tylko w roztworach
Slide 2
Substancje możemy podzielić na: elektrolity wodne roztwory tych substancji przewodzą prąd elektryczny (kwasy, zasady, sole) nieelektrolity ich wodne roztwory nie przewodzą prądu elektrycznego (cukier, alkohole)
Slide 3
Teoria dysocjacji elektrolitycznej dysocjacja samorzutny rozpad na jony Założenia: 1. Podczas rozpuszczania w wodzie niektórych substancji następuje ich samorzutny rozpad na jony dodatnie (kationy) i ujemne (aniony) 2. Powstające kationy i aniony mają wpływ na właściwości chemiczne roztworu 3. Nie wszystkie substancje w jednakowym stopniu rozpadają się na jony
Slide 4
Kwasy, zasady i sole wg Arrheniusa kwasy to substancje, które dysocjują na kationy wodorowe i H O aniony reszt H xkwasowych R xH R x zasady to substancje, które dysocjują na kationy metali i H O aniony wodorotlenowe Me(OH ) M n nOH 2 2 n sole to substancje, które H O dysocjują naMkationy mmetali n i mR n Rm nM aniony reszt kwasowych 2
Slide 5
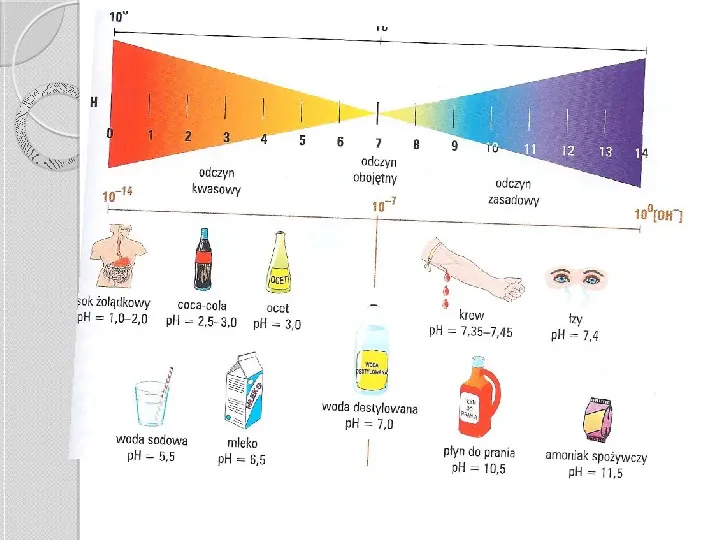
Odczyn roztworów wodnych roztwory kwasów mają odczyn kwaśny wywołany obecnością jonów H roztwory wodorotlenków (zasady) moją odczyn zasadowy wywołany obecnością jonów OHgdy stężenie jonów H i OH- są równe odczyn roztworu jest obojętny miarą kwasowości i zasadowości jest pH roztworu pH log H
Slide 7
Reakcje zobojętniania reakcje kwasów z zasadami łączenie kationów wodoru i anionów wodorotlenowych w niezdysocjowane cząsteczki wody Zadanie: 1. H OH H 2O Napisz równania reakcji zobojętniania kwasu fosforowego (V) zasadą sodową, kwasu siarkowego (VI) zasadą wapniową, kwasu solnego zasadą potasową. Podaj nazwy soli powstających w tych reakcjach.
Slide 8
Powinieneś: umieć napisać równania procesów dysocjacji kwasów, zasad i soli umieć nazwać powstające jony umieć za pomocą równań reakcji przedstawić przebieg dowolnej reakcji zobojętniania
Dane:
- Liczba slajdów: 8
- Rozmiar: 0.48 MB
- Ilość pobrań: 71
- Ilość wyświetleń: 5825