Zobacz slidy
Treść prezentacji
Slide 1
Analiza chemiczna instrumentalna Charakterystyka wartości metod
Slide 2
Zalety i wady analizy instrumentalnej Szybkość wykonania analizy Obiektywność pomiaru Łatwe do automatyzacji i komputeryzacji Duża czułość Porównawczy charakter oznaczenia Mniejsza dokładność Mniejsza precyzja oznaczenia Kosztowna aparatura
Slide 3
Podział metod instrumentalnych Na podstawie: - rodzaju obserwowanych zjawisk fizycznych lub fizykochemicznych; - sposobu ich wywołania; - rodzaju uzyskiwanej informacji pośredniej Metody optyczne Metody spektrochemiczne Metody elektrochemiczne Metody kinetyczne i metody rozdzielania Metody radiometryczne
Slide 4
Metody optyczne Metody oparte na sprężystych oddziaływaniach promieniowania elektromagnetycznego z próbką badaną. Oddziaływania te nie powodują zmiany ilości energii promieniowania. Zmienia się jego kierunek (fali, strumienia fotonów)
Slide 5
Techniki pomiaru intensywności zmętnienia Badanie bezbarwnych substancji nierozpuszczalnych. Intensywność zmętnienia jest wprost proporcjonalna do stężenia badanej substancji.
Slide 6
1. Nefelometria Obserwowane zjawisko - rozproszenie promieniowania. Pomiar - natężenie wiązki światła rozproszonego wychodzącego z kuwety pomiarowej (pod pewnym kątem w stosunku do światła wchodzącego. Zastosowanie - analiza chemiczna i analiza namnożenia komórek w hodowli, stężenie substancji, badanie stopnia dyspersji koloidu. 2. Turbidymetria Obserwowane zjawisko - rozproszenie (i absorpcja) promieniowania. Pomiar - zmniejszenie natężenia wiązki światła po przejściu przez kuwetę z zawiesiną. Zastosowanie - analiza chemiczna i analiza namnożenia komórek w hodowli.
Slide 7
- Testy rozpuszczalności - Immunoprecypitacja - Monitoring wzrostu bakterii i grzybów - Badanie leków - Oznaczanie masy cząsteczkowej makromolekuł
Slide 8
Technika pomiaru współczynnika załamania światła Ta sama substancja w różnych stężeniach oraz różne substancje w tym samym stężeniu wykazują różny współczynnik załamania światła (refrakcji - n).
Slide 9
1. Refraktometria Obserwowane zjawisko - załamanie światła. Pomiar - współczynnik załamania światła padającego na powierzchnię próbki Zastosowanie - oznaczanie stężenia substancji znanych, określenie składu mieszanin dwuskładnikowych o różnych n, określanie cech budowy cząsteczek związku chemicznego (refrakcja molowa RM), identyfikacja cieczy organicznych i minerałów, ocena jakości produktów. 2. Interferometria Obserwowane zjawisko - załamanie dwóch wiązek światła z tego samego źródła w dwóch badanych środowiskach. Pomiar - różnicy współczynników załamania światła w dwóch badanych ośrodkach.
Slide 10
Technika pomiaru polaryzacji światła i skręcenia płaszczyzny polaryzacji W wiązce światła spolaryzowanego drgania fali świetlnej są uporządkowane w jednej płaszczyźnie. Kąt skręcenia płaszczyzny polaryzacji jest proporcjonalny do stężenia substancji wywołującej skręcenie.
Slide 11
1. Polarymetria Obserwowane zjawisko - zdolność substancji optycznie czynnej (nie posiadającej elementów symetrii) do skręcania płaszczyzny światła spolaryzowanego. Pomiar - kąt skręcenia polaryzacji światła (alfa) Aparatura - polarymetr. Zastosowanie - identyfikacja i oznaczanie środków leczniczych, badanie równowagi i mechanizmów reakcji, ustalanie budowy przestrzennej związków złożonych (dyspersja skręcalności).
Slide 12
Technika pomiaru odbicia wiązki światła. Reflektometria służy głównie do pomiarów długości i tłumienności przewodów miedzianych, a także włókien światłowodowych, stosowanych w torach telekomunikacyjnych.
Slide 13
Metody spektroskopowe Dotyczą pomiaru zjawisk związanych z niesprężystym oddziaływaniem promieniowania elektromagnetycznego z badaną próbką. Podczas tego oddziaływania zachodzi wymiana energii zgodnie z regułami kwantowo optycznymi. Oparte są na technikach: absorpcyjnej i emisyjnej. W wyniku pomiarów powstają widma absorpcyjne lub widma emisyjne.
Slide 14
Techniki absorpcyjne Wykorzystują fakt zdolności niektórych substancji do pochłaniania światła. Substancje takie pochłaniają zwykle fale świetlne o określonych długościach w sposób charakterystyczny, zależny od budowy. Jeśli nawet pochłanianie zachodzi w tym samym zakresie długości fal, charakterystyczna pozostaje zwykle intensywność pochłaniania. W technikach tych stosuje się pomiar absorbancji (A), natężenia światła (I) oraz transmitancji (T).
Slide 15
A. Techniki absorpcyjne cząsteczek spektrofotometria, absorpcjometria Są zbiorem technik spektrofotometrii absorpcyjnej. W wyniku użycia aparatów zwanych spektrofotometrami uzyskuje się widma absorpcyjne, charakterystyczne dla badanej substancji. Przez badaną próbkę przechodzą kolejno wiązki światła monochromatycznego. Podział metod spektrofotometrycznych związany jest z określonym przedziałem długości fal świetlnych stosowanych i z różnorodnością ich oddziaływań niesprężystych z substancją badaną. Różne są również źródła promieniowania elektromagnetycznego.
Slide 16
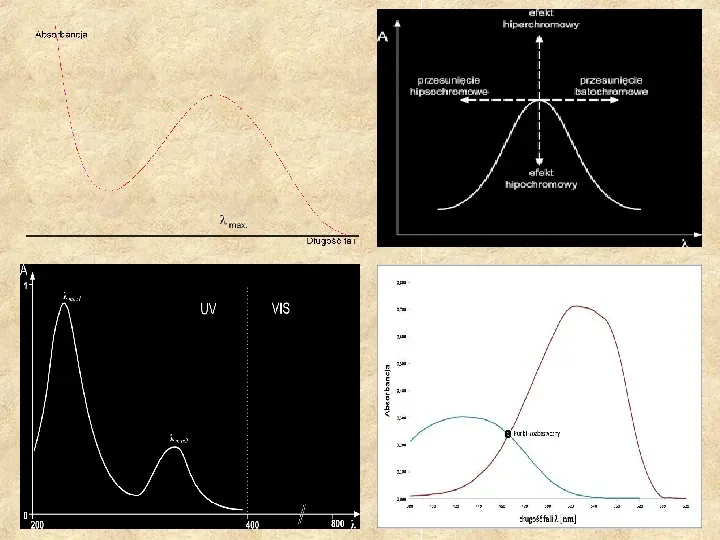
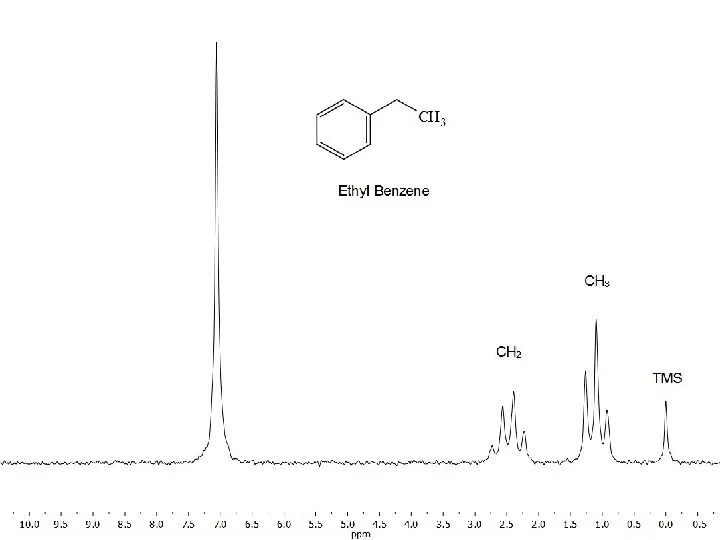
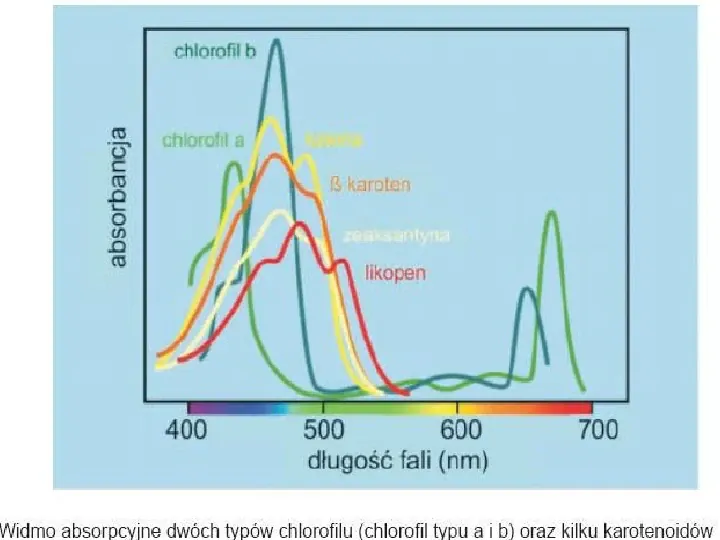
1. Spektrometria UVVIS Obserwowane zjawisko - absorpcja promieniowania ultrafioletowego i widzialnego w zakresach 200 400 nm i 400 750 nm związana ze zmiana stanów elektronowych oraz energii oscylacyjnej i rotacyjnej badanej cząsteczki. Efekt - widmo elektronowe (elektronowo oscylacyjno rotacyjne) z charakterystycznymi pasmami absorpcji. Źródło promieniowania lampy żarowe, deuterowe, rtęciowe. Aparat - spektrofotometr UV VIS Zastosowanie - analiza ilościowa, badanie mechanizmu i kinetyki reakcji chemicznych, identyfikacja związków bezbarwnych (aromatycznych, ketonów, estrów) w zakresie UV oraz barwnych w zakresie VIS.
Slide 19
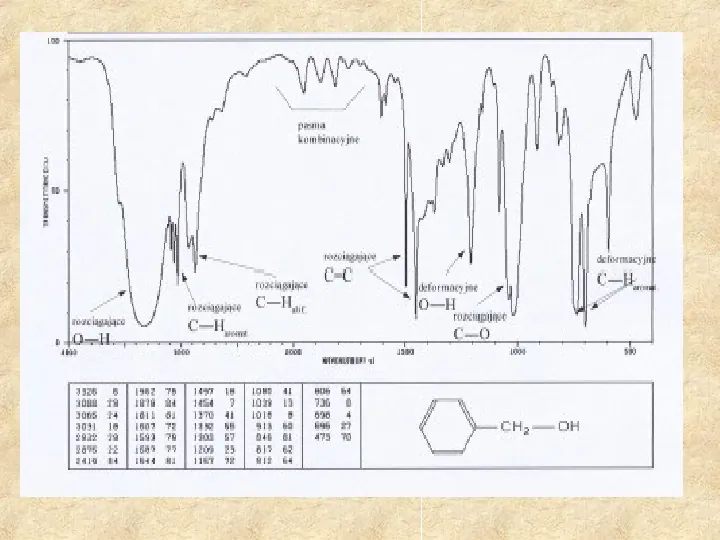
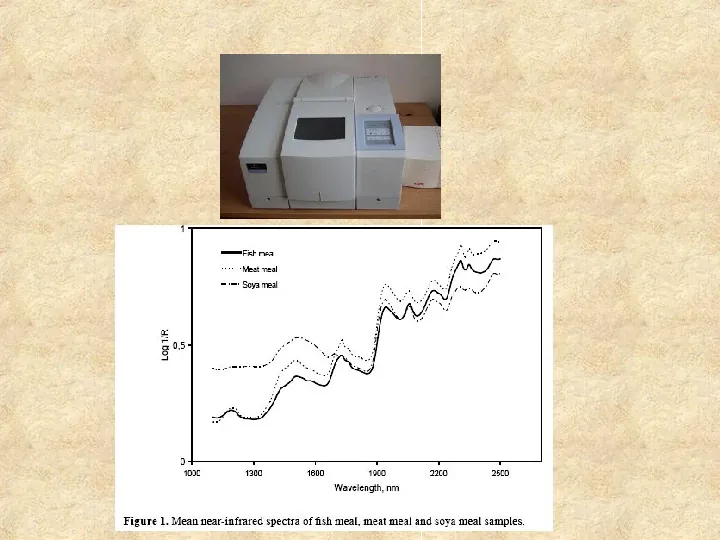
2. Spektroskopia w podczerwieni (IR) Obserwowane zjawisko - absorpcja promieniowania podczerwonego przez oscylujące cząsteczki w zakresie długości fal 0,2 30 mm. Grupy funkcyjne i charakterystyczne ugrupowania atomów absorbują specyficznie promieniowanie w wąskich przedziałach długości fal IR. bliska podczerwień (ang. near infrared, NIR) to zakres0,82,5 µm średnia podczerwień (ang. mid infrared, MIR) to zakres 2,525 μm daleka podczerwień (ang. far infrared, FIR) to zakres 251000 μm Efekt - widmo absorpcyjne o charakterystycznych dla obecnych ugrupowań liczbach falowych absorpcji. Aparat - spektrofotometr Fouriera (FTIR, NIR). Źródło promieniowania - włókno Nernsta (z tlenku cyrkonu) lub globar (z węglika krzemu) rozgrzane do temperatury 1000 1800oC. Zastosowanie - jedna z najlepszych metod identyfikacji struktur. Widmo w zakresie fal długich stanowi tzw. obszar daktyloskopowy.
Slide 22
Spektrometr NIR
Slide 24
3. Spektroskopia magnetycznego rezonansu jądrowego (NMR) Obserwowane zjawisko - absorpcja promieniowania w zakresie fal radiowych 1 3000 m przez jądra atomów cząsteczki w polu magnetycznym o dużym natężeniu. Efekt - widmo sygnałów rezonansowych próbki na skali przesunięć chemicznych. Aparat - spektrometr NMR. Źródło promieniowania - obwody elektroniczne, kryształy. Zastosowanie - badanie struktur cząsteczek.
Slide 25
Spektrometr NMR
Slide 27
4. Spektroskopia paramagnetycznego rezonansu elektronowego (EPR) Obserwowane zjawisko -absorpcja promieniowania mikrofalowego przez rotujące cząsteczki. Długość fali promieniowania 3 300 mm. Efekt - widmo rezonansowe. Aparat - spektrometr EPR. Źródło promieniowania klistron, magnetron. Zastosowanie - identyfikacja struktur.
Slide 28
5. Absorpcjometria kolorymetria Obserwowane zjawisko absorpcja światła w zakresie widzialnym przez substancje barwne z pomiarem absorpcji lub intensywności zabarwienia. Pomiar - absorbancja (A). Aparat - kolorymetr to uproszczony spektrofotometr. Zastosowanie - oznaczanie stężeń substancji barwnych na podstawie krzywej wzorcowej.
Slide 30
B. Techniki absorpcyjne atomów 1. Atomowa spektrometria absorpcyjna (ASA) Obserwowane zjawisko - absorpcja promieniowania elektromagnetycznego przez atomy cząsteczek w stanie pary wolnych atomów. Pomiar - absorbancja wprost proporcjonalna do liczby atomów w środowisku obserwowanym. Zakres promieniowania absorbowanego określa rodzaj pierwiastka. Źródło promieniowania - lampy z katodą wnękową, lampy bezelektrodowe. Zastosowanie - identyfikacja atomów 70 różnych pierwiastków.
Slide 31
2. Absorpcja rentgenowska Obserwowane zjawisko - absorpcja promieniowania w zakresie rentgenowskim. Długość fali 0,03 30 nm, przez atomy cząsteczki charakterystycznie dla ich rodzaju i niezależnie od budowy cząsteczki, w której się znajdują. Zjawisko związane jest z wybijaniem elektronu z powłoki wewnętrznej atomu, który ulega jonizacji. Pomiar - absorbancja. Źródło promieniowania - lampa rentgenowska. Aparat - fotometr absorpcji rentgenowskiej. Zastosowanie - oznaczanie atomów pierwiastków ciężkich w próbce.
Slide 32
Techniki emisyjne Pojedyncze atomy, cząsteczki pierwiastków oraz związków chemicznych obdarzone są pewnym zasobem energii wewnętrznej, której ilość ulega zmianie. Stany podwyższonej energii są nietrwałe. Następuje emisja nadmiaru energii aż do stanu minimalnej dla danych warunków wartości. Atomy poddane wzbudzeniu emitują widmo liniowe (wybrane długości fal promieniowania). Emisja promieniowania następuje przy przejściu ze stanu wzbudzonego na niższy poziom energii. Techniki emisyjne dzieli się w zależności od rodzaju wzbudzenia, od którego zależy ilość pochłoniętej energii i stopień wzbudzenia. Inny podział dotyczy rodzaju źródła emisji.
Slide 33
A. Techniki emisyjne atomowe 1. Fotometria płomieniowa Obserwowane zjawisko - emisja promieniowania przez atomy próbki po atomizacji i wzbudzeniu w strumieniu energii. Źródło energii - płomień palnika temperatura do 3.500 K. Aparat - fotometr płomieniowy Zastosowanie - badanie zawartości pierwiastków łatwo wzbudzanych (sód, potas), składu wody, płynów ustrojowych i ekstraktów roślinnych.
Slide 34
2. Spektrometria emisyjna Obserwowane zjawisko - emisja promieniowania UV - VIS Źródło energii - plazma (zjonizowany gaz obojętny elektrycznie) 400010000 K. Aparat - spektrometr emisyjny. Pomiar - bezpośredni pomiar natężenia emitowanego promieniowania Zastosowanie - badania pierwiastków śladowych. Aparatura bardzo droga, tylko do oznaczeń seryjnych.
Slide 35
3. Fluorescencja rentgenowska Obserwowane zjawisko - emisja promieniowania rentgenowskiego przez elektron przechodzący z powłoki zewnętrznej na miejsce wybitego promieniowania fluorescencyjnego Źródło energii - lampa rentgenowska. Aparat - fluorescencyjny spektrometr rentgenowski. Efekt - widmo fluorescencyjne niezależne od rodzaju związku. Zastosowanie - Analiza śladowa
Slide 36
B. Techniki emisyjne cząsteczkowe Substancje chemiczne podlegające napromieniowaniu ulegają wzbudzeniu, a następnie emitują pochłoniętą energię w postaci promieniowania elektromagnetycznego lub w postaci ciepła. Substancje te często powodują emisję światła w zakresie widzialnym. Mechanizm przejść elektronowych decyduje o tym czy jest to fluorescencja czy fosforescencja. Oba zjawiska nazywane są ogólnie luminescencją. Rodzaje luminescencji fotoluminescencja cząsteczki wzbudzone promieniowaniem elektromagnetycznym chemiluminescencja cząsteczki wzbudzone w czasie reakcji chemicznej bioluminescencja wzbudzenie cząsteczek w przebiegu procesów biologicznych elektroluminescencja wzbudzenie strumieniem elektronów.
Slide 37
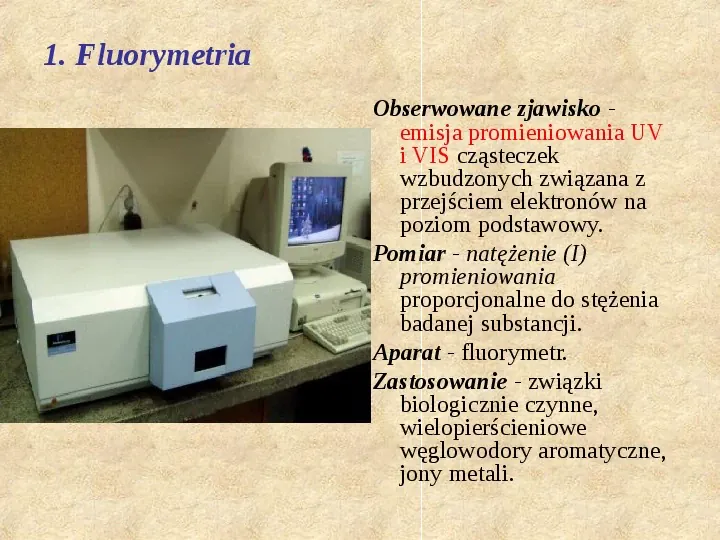
1. Fluorymetria Obserwowane zjawisko emisja promieniowania UV i VIS cząsteczek wzbudzonych związana z przejściem elektronów na poziom podstawowy. Pomiar - natężenie (I) promieniowania proporcjonalne do stężenia badanej substancji. Aparat - fluorymetr. Zastosowanie - związki biologicznie czynne, wielopierścieniowe węglowodory aromatyczne, jony metali.
Slide 38
Metody elektrochemiczne Wykorzystują one zjawiska związane z przepływem prądu elektrycznego przez roztwory elektrolitów i reakcje zachodzące na elektrodach zanurzonych w roztworach elektrolitów.
Slide 39
A. Metody potencjometryczne Oparte na pomiarze różnicy potencjałów elektrochemicznych między elektrodami zanurzonymi w analizowanych roztworach (elektroda wskaźnikowa i elektroda odniesienia). Potencjał elektrody wskaźnikowej zależy od stężenia badanej substancji. Potencjometria bezpośrednia Różnica potencjałów między elektrodami zależy wprost od stężenia substancji badanej.
Slide 40
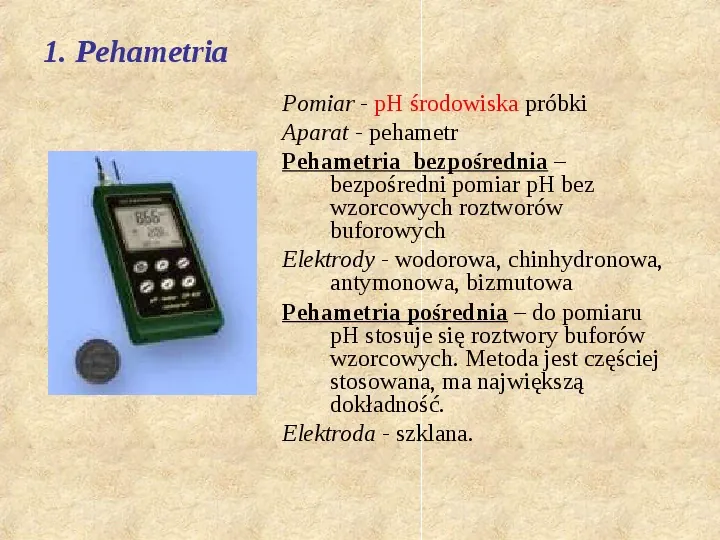
1. Pehametria Pomiar - pH środowiska próbki Aparat - pehametr Pehametria bezpośrednia bezpośredni pomiar pH bez wzorcowych roztworów buforowych Elektrody - wodorowa, chinhydronowa, antymonowa, bizmutowa Pehametria pośrednia do pomiaru pH stosuje się roztwory buforów wzorcowych. Metoda jest częściej stosowana, ma największą dokładność. Elektroda - szklana.
Slide 41
2. Miareczkowanie potencjometryczne Pomiar - zmiana potencjału w zależności od objętości zużytego odczynnika miareczkującego, określenie punktu końcowego miareczkowania. Miareczkowanie pehametryczne Elektrody - szklana, chinhydronowa, wodorowa Miareczkowanie redoksymetryczne Elektrody - wskaźnikowa platynowa; odniesienia NEK (nasycona elektroda kalomelowa) Miareczkowanie precypitometryczne Elektrody - z metali biorących udział w oznaczeniu Miareczkowanie kompleksometryczne Elektrody - jonoselektywna, rtęciowa
Slide 42
B. Metody elektrolityczne Polegają na pomiarze (ważeniu) wydzielonego, oznaczanego składnika roztworu, na elektrodzie podczas przepływu prądu elektrycznego pomiędzy elektrodami w nim zanurzonymi. Obserwowane zjawisko - elektroliza w całej masie Pomiar - masa substancji wydzielonej na elektrodzie.
Slide 43
1. Elektrograwimetria (elektroliza) Elektroda - katoda platynowa Zastosowanie - do oznaczania ilościowego pojedynczych substancji (metali) 2. Elektroliza wewnętrzna Elektroda - ogniwo galwaniczne (elektrody platynowa i cynkowa połączone przewodem) Na elektrodzie platynowej wydziela się metal znajdujący się w roztworze, do roztworu przechodzi zaś ilościowo cynk z drugiej elektrody.
Slide 44
Metody kulometryczne W przebiegu oznaczenia zachodzi zjawisko elektrolizy w całej masie badanej próbki Pomiar - ładunku elektrycznego (C) przepływającego przez badany roztwór elektrolitu, niezbędnego do reakcji elektroutlenienia i elektroredukcji oznaczanej substancji. Wartość ładunku zmierzonego jest proporcjonalna do zawartości. 1. Analiza kulometryczna bezpośrednia Substancja badana podlega reakcji bezpośredniej na elektrodzie. 2. Analiza kulometryczna pośrednia Substancja reaguje z inną, wytwarzaną na elektrodzie
Slide 45
Metody z pomiarem przewodnictwa lub pojemności elektrycznej 1. Konduktometria Obserwowane zjawisko - przewodnictwo (konduktancja mierzona w simensach S) roztworów elektrolitów, zależna od stężenia, ładunku i rozmiaru jonów. Pomiar - przewodność elektrolitu Aparatura - konduktometr 2. Oscylometria z miareczkowaniem oscylometrycznym Obserwowane zjawisko - przewodnictwo roztworów elektrolitów, zależna od stężenia, ładunku i rozmiaru jonów. Pomiar - przewodność pozorna (admitancja), jako odwrotność pozornej rezystancji (impedancji). Pomiar bezprzewodowy z wykorzystaniem prądu o dużych częstotliwościach Aparatura - oscylometr pojemnościowy, oscylometr indukcyjny.
Slide 46
Metody woltamperometryczne Oparte są na pomiarze natężenia prądu elektrycznego przepływającego w układzie elektrod w roztworze badanym pod wpływem przyłożonego napięcia. Pomiar dokonywany jest z użyciem rtęciowej elektrody kroplowej. 1.Polarografia Rodzaje stało-; zmiennoprądowa; pulsowa; oscylopolarografia. Obserwowane zjawisko - elektroliza warstwy dyfuzyjnej. Pomiar - natężenie prądu, jako funkcja przyłożonego napięcia, proporcjonalnego do stężenia Aparatura - polarograf. 2. Woltamperometria Pomiar - zależność natężenia prądu od napięcia przyłożonego do elektrod. Zastosowanie - analiza śladowa, materiałów roślinnych, preparatów farmaceutycznych
Slide 47
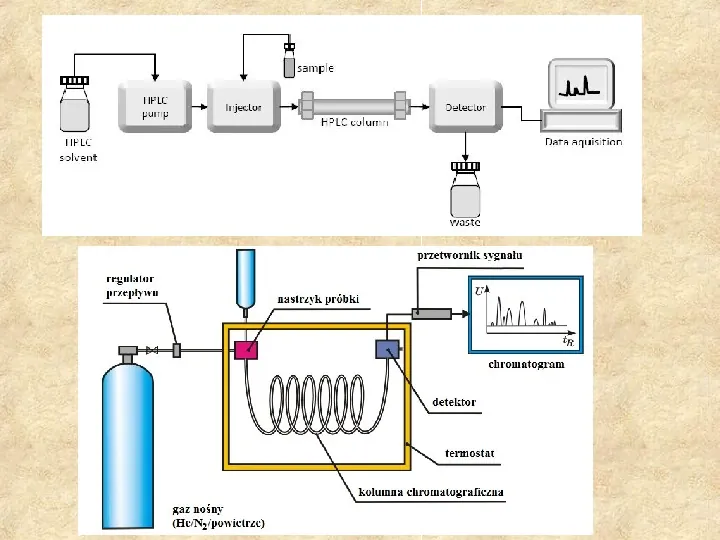
Metody rozdzielcze Służące wyizolowaniu substancji, jej identyfikacji i oznaczaniu, dzięki zróżnicowanej odpowiedzi specyficznych substancji na warunki rozdziału. 1.Elektroforeza Zjawisko - zróżnicowana szybkość poruszania się naładowanych cząstek mieszaniny w polu elektrycznym. Parametr podziału - ruchliwość elektroforetyczna m Rodzaje - swobodna; w nośnikach; na bibule; na żelach; kapilarna. Zastosowanie - bardzo szerokie w analityce medycznej. 2. Chromatografia Zjawisko - podział składników mieszaniny pomiędzy fazę stacjonarną i ruchomą układu parametry podziału - współczynnik retencji (k); ułamek czasu migracji substancji (Rf) czynnik zatrzymania lub ułamek prędkości; RM log k Rodzaje - ch. Gazowa; cieczowa, kolumnowa; cienkowarstwowa.
Slide 48
Chromatograf HPLC i GC-MS
Slide 50
Metody radiometryczne Polegają na pomiarze promieniowania jądrowego emitowanego przez naturalne i sztuczne izotopy promieniotwórcze. Również efekty naświetlania badanej próbki promieniowaniem jądrowym. Metody oparte na absorpcji i odbiciu promieniowania jądrowego. Metody oparte na pomiarze aktywności naturalnych pierwiastków promieniotwórczych. Metody aktywacji. Metody polegające na wzbudzeniu atomów przez naświetlanie promieniowaniem g ze źródeł izotopowych. Metody wskaźników promieniotwórczych.
Dane:
- Liczba slajdów: 50
- Rozmiar: 1.22 MB
- Ilość pobrań: 195
- Ilość wyświetleń: 10048