Zobacz slidy
Treść prezentacji
Slide 1
ESPORT Forma rywalizacji, w której przedmiotem działań zawodników są gry komputerowe. Rywalizacja między zawodnikami (graczami) odbywa się zarówno w formie rekreacyjnej, jak i na turniejach gier komputerowych (tzw. pro gaming). Na świecie działają objęte prestiżem turnieje takie jak World Cyber Games (WCG) i Electronic Sports World Cup (ESWC), a w Polsce Poznań Game Arena (PGA) oraz Electronic Sports League (ESL). Poszczególne gry komputerowe różnych gatunków, w których toczy się rozgrywka między zawodnikami, są nazywane dyscyplinami.
Slide 2
Mecze rozgrywane są na żywo, a publiczność może oglądać graczy siedzących przed komputerami, zaś ich posunięcia śledzić na wielkich telebimach. Rozgrywki w internecie są wykorzystywane częściej przy eliminacjach. Formuła sportu elektronicznego przyciąga coraz większe rzesze graczy w wieku od kilku do kilkudziesięciu lat, głównie dzięki niwelowaniu barier fizycznych, spotykanych w
Slide 3
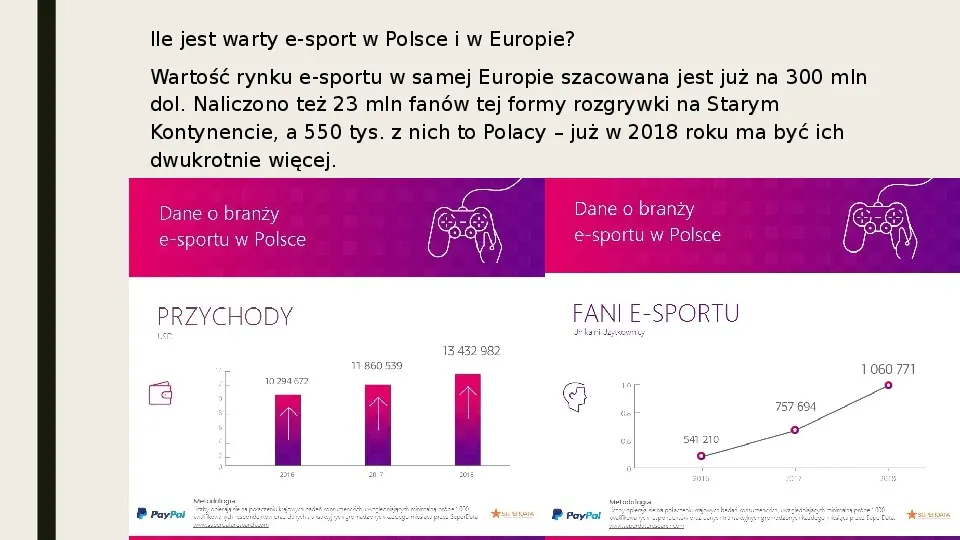
Ile jest warty e-sport w Polsce i w Europie? Wartość rynku e-sportu w samej Europie szacowana jest już na 300 mln dol. Naliczono też 23 mln fanów tej formy rozgrywki na Starym Kontynencie, a 550 tys. z nich to Polacy już w 2018 roku ma być ich dwukrotnie więcej.
Slide 4
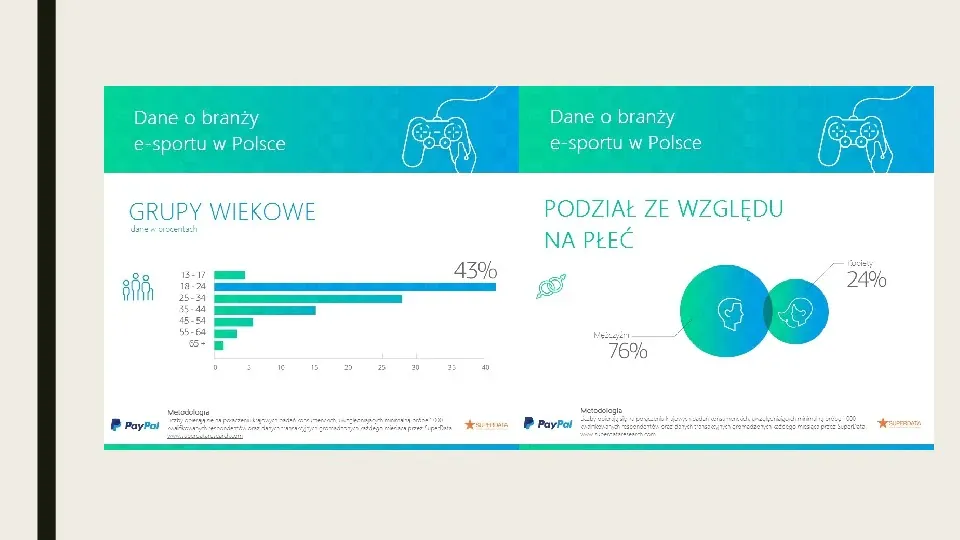
Co ciekawe, odsetek fanów e-sportu wśród europejskich państw jest najwyższy w Polsce. Te liczby to dowód na to, że e-sport wyszedł już z niszy, a w przeciągu najbliższych lat ma szansę jeszcze urosnąć przynosząc jeszcze więcej pieniędzy także w naszym kraju. Przeciętny gracz jest zwykle mężczyzną w wieku od 18 do 34 lat i przynosi rocznie średnio 13,3 dol. przychodów branży. W przypadku polskich kibiców kobiet jest jednak zdecydowanie więcej niż w innych europejskich państwach w Rosji i Hiszpanii jest to odpowiednio 15 proc. i 13 proc. wszystkich fanów, natomiast w Polsce aż 24. Polska wyróżnia się też na innym tle. Okazuje się, że wbrew pozorom najmłodsi fani wcale nie są główną grupą kibiców. Największa grupa 43 proc. mieści się w przedziale od 18 do 24 lat. Tylko 3 proc. jest w wieku od 13 do 17 lat, a w innych krajach osoby w tym wieku to kilkanaście procent kibiców.
Slide 6
Sub-rynek eSportu to jedna z najszybciej rozwijających się gałęzi interaktywnej rozrywki. Między 2016 i 2019 rokiem wartość tego rynku ma przekroczyć magiczną barierę 1 miliarda dolarów. To najlepsza okazja, aby zajrzeć do portfeli eSportowców. Szybkiego, czytelnego podsumowania pod tytułem Kto i gdzie zarabia na eSporcie? dostarczyła nam agencja Mindspot. W takim razie sprawdźmy, gdzie najbardziej opłaca się zarywać noce przed CS:GO i LoL-em, szlifując eSportowe umiejętności. Na początek informacja, która pokaże nam kontekst całej sytuacji. Do 2019 roku światowy rynek eSportu będzie wart aż 1,1 mld dolarów! Dokonując bezsensownego porównania, to więcej, niż polskie rynki hotelarskie, SPA i lodowe razem wzięte.
Slide 7
Jeżeli chodzi o nasze, polskie podwórko, aktualną wartość eSportowego rynku szacuje się na 40 milionów złotych. To mniej więcej tyle, ile zarobili polscy piłkarze za występy podczas EURO 2016. A będzie tylko lepiej. Zaskoczeniem może być fakt, że łączne przychody z eSportu są u nas wyższe niż w Azji! Stary Kontynent nie przegonił jednak USA, które wiedzie prym w komercjalizacji eSportowego fenomenu. Zupełnie mnie to nie dziwi. Pozostając na chwilę w katowickim Spodku, warto przypomnieć sobie największą odnotowaną wygraną polskich eSportowców. Doskonale znana, popularna ekipa Virtus.pro zgarnęła 1,5 miliona złotych, wygrywając w CS:GO finały ligowe. A rodzice mówili, że z grania nie będzie pieniędzy
Slide 8
Jeżeli chodzi o największe wygrane na świecie, niepokonana zostaje Dota 2. Współfinansowanie nagrody przez fanów gry, którzy kupują przedmioty wewnątrz cyfrowego sklepu, pozwoliło w 2016 roku przeznaczyć aż 20 milionów dolarów na nagrody turnieju The International. Tylko jeden milion z tej sumy wyłożyli organizatorzy. W zeszłym roku IEM w Katowicach odwiedziło 100 tys. osób, to dwa razy więcej niż obserwowało skoki na Wielkiej Krokwi w Zakopanem. Przed swoimi komputerami mistrzostwa śledziło zaś w jednym momencie nawet 1 mln osób, czyli prawie tyle ile ogląda Tour de Pologne na Jedynce. IEM 2015 był wielki. Dziesiątki tysięcy odwiedzających, światowej sławy gracze, cosplayerki i cosplayerzy, a także jutuberzy.
Slide 9
Zaledwie kilkanaście dni temu rozpisywałem się nad potencjałem e-sportu. Powodem rozważań było wejście do cyfrowego świata globalnych marek takich jak Coca-Cola, American Express czy Nissan. Dzisiaj dokonał się kolejny krok utwierdzający mnie w przekonaniu o świetlanej przyszłości profesjonalnych rozgrywek komputerowych. Od teraz każdy z nas może obstawiać wyniki ulubionych drużyn w takich grach jak Dota 2 oraz StarCraft II Obstawianie wyników meczy w Counter-Strike, League of Legends czy innym StarCrafcie dla wielu miłośników e-sportu wcale nie jest czymś odkrywczym. Chociaż w Polsce do wczoraj było to egzotyką, przyjmowanie zakładów na największych zagranicznych portalach bukmacherskich jest już normą. Wielu moich znajomych właśnie tam oddawało swoje ciężko zarobione pieniądze, silniej i silniej dając się obejmować mrocznym mackom hazardu.
Slide 10
Odkładając jednak żarty na bok, od teraz e-sport stał się częścią oferty zakładów sportowych STS. Jak wielu z was może wiedzieć, Star-Typ Sport to lider tego typu usług w naszym kraju, który działa nieprzerwanie od 1997 roku. Legalny bukmacher posiada 400 placówek do przyjmowania zakładów oraz zatrudnia ponad 1000 osób. To nie jest żadna podwórkowa firma, tylko potężna machina, która stara się docierać do coraz to nowych i nowych grup klientów.
Slide 11
Młodzi gracze pod pseudonimami Dade, Cool czy Mata to idole młodego pokolenia, tak jak dla nas idolami był Beckham i Zidane. Chociaż rozsiadający się przed komputerami gracze nie są zbyt emocjonującym widokiem, tak już wydarzenia w świecie gry potrafią rozpalić do czerwoności dziesiątki tysięcy widzów. Kto był na finałach Inter Extreme Masters w katowickim Spodku, ten zresztą wie to najlepiej.
Slide 12
Nie tylko przez samych graczy, ale również poważne firmy, które widzą w tym obszarze rosnący potencjał. Star-Typ Sport to tylko jeden z podmiotów. Wcześniej Polsat Viasat Explore emitował esportowe rozgrywki. Miesiąc Temu katowicka Rada Miasta przyjęła uchwałę o wsparciu organizacji Intel Extreme Masters. AMD finansuje polską drużynę Roccat, z kolei z nieoficjalnym informacji wiem, że do wejścia w obszar e-sportu przymierza się znany polski ba W Polsce eSport nigdy nie należał do najbardziej popularnych dyscyplin. Co więcej, bardzo ciężko nam stwierdzić, czy godziny spędzone przed PC można nazwać sportową dyscypliną. W nadwiślańskim ludzie zaszły jednak wielkie zmiany, głównie za sprawą tytułu, który albo się kocha, albo nienawidzi League of Legends. Dzięki niemu setki tysięcy młodych ludzi, również w Polsce, zaczęły traktować gry komputerowe nie jako rozrywkę, ale szansę wybicia się, sprawienia sobie lepszego życia, za pomocą myszki i klawiatury.
Slide 13
Rodacy odnoszą wiele sukcesów na eSportowej scenie, wygrywając wielotysięczne nagrody oraz będąc znacznie bardziej rozpoznawalni za granicą, niż we własnych włościach. Turnieje turniejami, co jednak z normalną prozą życia? Poza grami i treningami trzeba mieć przecież standardowo rozumianą pracę, pozwalającą na utrzymanie siebie, nie raz swojej rodziny, zakup sprzętu oraz wysokiej jakości urządzeń peryferyjnych. No właśnie sęk w tym, że nie trzeba. Wystarczy dobrze grać w League of Legends. Miesięczna pensja na średnim poziomie 9 tysięcy złotych powinna zadowolić większość z waszych portfeli, prawda? Nie musisz być najlepszy Nie musisz być najlepszy, aby tyle zarabiać. Nie musisz być mistrzem, wieloletnim czempionem danego tytułu. Wyżej wymieniona pensja to miesięczna stawka za granie naszego rodaka, Jakuba Creotana Grzegorzewskiego. Jakub należy do zespołu Alternate Attax i wraz z 7 innymi drużynami ubiega się o puchar rozgrywek League of Legends Championsip Series. Zgadza się, tej samej imprezy, dzięki której rząd Stanów Zjednoczonych wprowadził zmiany do swojej polityki wizowej.
Slide 14
Jakub nie jest więc żadnym królem LoLa, nie posiada takiej sławny i marki jak inni gracze, z niemal boskim Carlosem Ocelote Rodriguezem na czele. Swoją drogą, Alternate Attax wygrywa z SK Gaming, do którego należy Ocelote, 2 do 1, także fani eSportowych zmagań na pewno nie narzekają na brak wrażeń. Jak wygląda przeciętny dzień Jakuba? Wbrew pozorom, nikt nie zmusza go do wysiadywania po kilkanaście godzin dziennie przed komputerem, szlifując umiejętności oraz odparzając pośladki. Jak przyznaje Creaton, codzienne treningi całej grupy, trwające od 3 do 5 godzin, to maksimum wymaganego czasu spędzonego przed komputerem. Później co prawda można ćwiczyć dalej, ale już samemu. Każdy członek drużyny ceni swój wolny czas. Polak korzysta wtedy z basenu oraz bieżni. W zdrowym ciele zdrowy duch. Odpowiedni duch walki z kolei na pewno przyda się Jakubowi, widząc zainteresowanie oraz ogrom imprezy takiej jak Championship Series.
Slide 15
Alternate Attax ćwiczy wspólnie, w jednym miejscu, w jednym pomieszczeniu, będąc stale w kontakcie. Zlokalizowany na terenie NiemiecGaming house to miejsce, w którym ustalają taktyki, rozgrywają tak zwane stałe fragmenty gry, analizują przeciwnika oraz szlifują umiejętności. To w zasadzie tyle. Za całą resztę, taką jak drużynowy kontakt z mediami, rejestrowanie na turnieje, wyjazdy, wyloty, hotele i organizację, odpowiada manager zespołu. Poza managerem obecny jest również trener, który koordynuje postępy całej drużyny oraz pojedynczych jej członków. Też macie wrażenie, jak gdybym przestał pisać o graczach, zaczął natomiast o profesjonalnych piłkarzach wysokiej klasy? Poza samą pasją, samą formą sportu, nie ma tutaj wielkich różnic. W obu przypadkach turniejowych graczy oglądają tysiące osób na widowni. Tutaj i tutaj zawodnicy są obklejeni logami sponsorów, Adidasa i Biedronkę zamieniając na Intela oraz AMD. W Alternate Attax również dochodzi do wzniosłych przemówień na moment przed wyjściem do publiczności, na scenę. Zawodnicy mają swoje przyzwyczajenia, rytuały wręcz, bez których nie mogą się obejść. Różnice pojawiają się wtedy, kiedy Jakub Grzegorzewski powróci, z tarczą bądź na tarczy, do Polski. Na lotnisku nie będą czekać na niego zawstydzone fanki, piszczące w niebogłosy, prosząc o autograf. Z drugiej strony, nawet ta praktyka się zmienia. Jak przyznaje Creaton, z prośbą o autograf spotyka się coraz częściej. Coraz częściej jest również twarzą rozpoznawalną na ulicy, nie tylko w najbliższych kręgach.
Slide 16
Co trzeba zrobić, aby żyć z uprawiania eSportu? Jakub mówi o dwóch latach nieustannej gry, od dwóch do pięciu godzin dziennie przed komputerem grając w różnych turniejach I ligach. Po takim czasie po Creatona zgłosili się najlepsi, widząc jego poczynania. Dzięki temu dzisiaj 19-latek doskonali swoje umiejętności w Niemczech, obwieszony darmowym sprzętem, darowanym mu przez sponsorów, wyposażony w solidną stawkę za miesiąc treningów, która wzrasta do 15 tysięcy złotych w zależności od turniejowych rezultatów. Tych z kolei, patrząc na wyniki Alternate Attax, nie można młodym ludziom odmówić. Tradycyjny sport oraz eSportowe zmagania dzieli jeszcze jedna, lecz fundamentalna różnica. Piłka nożna, hokej czy koszykówka, kariera sportowców jest uzależniona tylko i wyłącznie od ich umiejętności, siły, zdrowia. W przypadku eSportu sprawa jest o wiele prostsza.
Slide 17
Kolejny przykład na to, że Polska e-sportem stoi. Klub Legia Warszawa organizuje pierwszy na świecie turniej gier wideo, w którym zmierzą się oficjalne e-drużyny prawdziwych klubów piłkarskich! Na całym świecie krystalizuje się trend posiadania oficjalnych e-drużyn prawdziwych klubów sportowych. Swoich e-odpowiedników posiada Manchetser United i masa innych profesjonalnych, pierwszoligowych zespołów. Ligapierwszego Mistrzów zobowiązuje, więc własnej eTo właśnie Legia Warszawa będzie gospodarzem turnieju e-drużyn kadry doczekała się również Legia Warszawa. europejskich klubów. Podczas Legia eSports Cup 2016 zmierzą się ze sobą najlepsi wirtualni piłkarze z całej Europy, oficjalnie reprezentowani barwami najlepszych piłkarskich klubów Starego Kontynentu. Drużyny najpierw zmierzą się w systemie każdy z każdym. Następnie rozpocznie się faza finałowa w systemie pucharowym przegrany odpada z dalszej rywalizacji. Łączna pula nagród wygospodarowana dla turnieju Legia eSports Cup 2016 wyniesie z kolei 15 000 złotych.
Slide 18
Niewiele, w porównaniu do innych e-sportowych mistrzostw, ale od czegoś trzeba zacząć. Co ciekawe, włodarze Legii wciąż nie podali tożsamości członków polskiego teamu. Organizatorzy chcą trzymać je w tajemnicy do samego końca. Już od dawna wiedzieliśmy, że Polacy kochają e-sport. Teraz mamy na to twarde dowody. ESL, największa na świecie firma zajmująca się e-sportem, sprawdziła, z jakich krajów pochodzą widzowie największych turniejów e-sportowych, czyli finałów Intel Extreme Masters oraz finałów ESL One. Okazuje się, że w bieżącym roku Polacy są w zdecydowanej czołówce narodów oglądających wirtualne rozgrywki. Aż 2,8 mln widzów pochodzących z naszego kraju oglądało finał Intel Extreme Masters 2016, co przełożyło się aż na 8 proc. całej widowni tych rozgrywek. Dwa lata wcześniej, w 2014 roku, te same rozgrywki e-sportowe oglądało ponad trzy razy mniej, a konkretnie 831 tys. Polaków.
Slide 19
Wtedy jednak e-sport cieszył się zdecydowanie mniejszą popularnością niż obecnie, więc taka liczba oglądających przełożyła się na 5,9 proc. wszystkich widzów. Widać tu zatem ogromny, wynoszący aż 340 proc., wzrost oglądalności względem poprzednich lat. W Stanach Zjednoczonych i Niemczech, pierwszym i drugim e-sportowym rynku świata, wzrosty te były mniejsze i wyniosły kolejno 264 i 200 proc. TOP 5 krajów, z których pochodzili widzowie turnieju IEM Katowice 2016: USA 19,7 (7 mln) Niemcy 8,1 (2,86 mln) Polska 8 (2,82 mln) Szwecja 5,7 (2 mln) Wielka Brytania 5 (1,8 mln)
Slide 20
Ogromne zainteresowanie Polaków finałami Intel Extreme Masters 2016 można oczywiście tłumaczyć tym, że od kilku lat impreza ta odbywa się w Polsce i jest lokalnie bardzo mocno promowana, także przez Spiders Web. W ten sposób nie da się jednak wyjaśnić zainteresowania finałami turnieju ESL One odbywającego się w Kolonii. W ciągu ostatnich trzech lat zainteresowanie tą imprezą w Polsce wzrosło aż 25-krotnie. W 2014 roku zawody te oglądało 99 tys. Polaków, zaś w 2016 roku liczba ta wzrosła aż do 2,5 mln. Także w przypadku tego wydarzenia wzrost był szybszy niż w USA oraz Niemczech. W Stanach Zjednoczonych liczba widzów wzrosła 13-krotnie (z ok. 450 tys. do ok. 5,8 mln), zaś w Niemczech 14-krotnie (z 191 tys. do 2,6 mln)
Slide 21
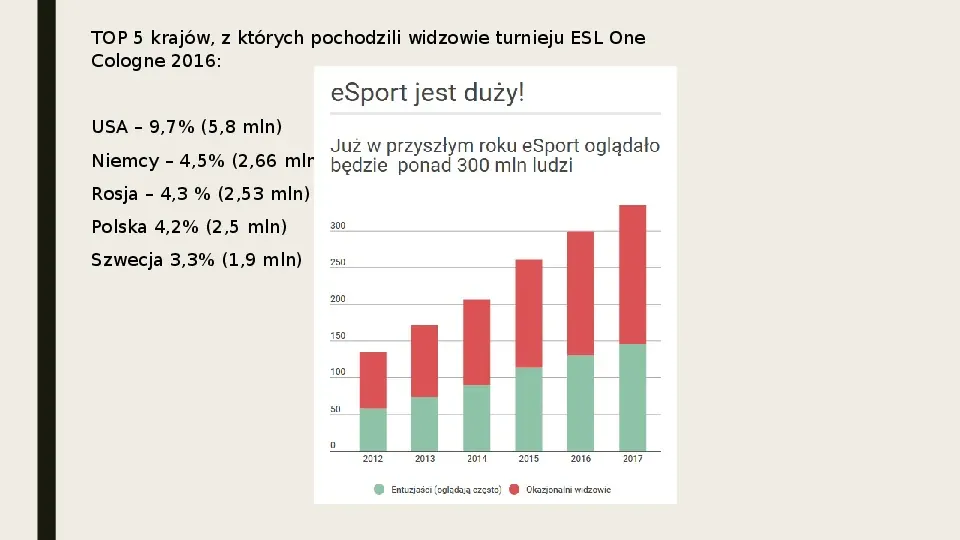
TOP 5 krajów, z których pochodzili widzowie turnieju ESL One Cologne 2016: USA 9,7 (5,8 mln) Niemcy 4,5 (2,66 mln) Rosja 4,3 (2,53 mln) Polska 4,2 (2,5 mln) Szwecja 3,3 (1,9 mln)
Slide 22
Należy podejrzewać, że ten stan rzeczy się utrzyma, a znaczenie e-sportu nadal będzie rosnąć. ESL szacuje, że w 2016 roku wartość rynku esportowego w Polsce wyniesie 40 mln zł, zaś w 2018 roku sięgnie aż 52 mln zł. Nie są to liczby porównywalne chociażby z piłką nożną czy siatkówką, to prawda. Jednak jeżeli ten stan rzeczy utrzyma się przez dłuższy czas, być może za kilkanaście lat poczynaniami naszych esportowych zawodników będziemy się emocjonować bardziej niż Mistrzostwami Europy lub Świata w piłce nożnej.
Slide 23
E-sportowym rozgrywkom można kibicować, można z nich kpić bądź mieć je całkowicie w nosie, ale nie sposób kłócić się z twardymi danymi. Te wskazują na kolejne rekordy i kolejne wielkie sumy, jakie padają w światku profesjonalnych graczy. Wirtualny sport na dorobku, jak słusznie nazywają rozgrywki tego typu sceptycy, stale rośnie, puchnie i rozlewa się na coraz większą liczbę potencjalnych odbiorców. Zwraca to uwagę nie tylko socjologów, graczy i osób piszących o interaktywnej rozgrywce, ale również ogromnych firm, które zaczynają przedkładać tradycyjne, narodowe zmagania na rzecz e-sportu. To, co przyciąga międzynarodowych gigantów do pasjonatów grających w StarCrafta II, League of Legends czy Counter Strike to właśnie globalność, rokująca lepiej niż najbardziej emocjonujący sezon NBA czy najlepsze mistrzostwa FIVB.
Slide 24
Mistrzostwa The International 2014 skupione wokół gry Dota 2 oglądało za pośrednictwem Internetu ponad 20 milionów osób. Poniedziałkowy finał rozgrywek widziały 2 miliony graczy. Zwycięska drużyna Newbee zdobyła 5 milionów dolarów, czyli mniej więcej połowę 10-milionowej puli przeznaczonej na nagrody. Dla porównania, premia ligi siatkowej FIVB dla polskich mistrzów świata wynosi 150 tysięcy dolarów, natomiast rewelacyjni siatkarze mogą jeszcze liczyć na minimum 3 miliony złotych od PZPS. The International 2014 to i tak nie największe widowisko poświęcone e-sportowi. Finały ligi League of Legends oglądało ponad 32 miliony widzów, z kolei emitowany w sieci finał zobaczyło 8,5 miliona graczy. Jestem ciekaw, o ile większy byłby to wynik, gdyby któraś z amerykańskich stacji telewizyjnych odważyłaby się emitować rozgrywki na swoim kanale, odpowiednio je wcześniej reklamując. Gdyby znalazł się sponsor, który byłby w stanie połączyć nowoczesny świat internetowego e-sportu z tradycyjną, telewizyjną formułą, ten zmieniłby całą branżę. To z kolei może się stać już niedługo.
Slide 25
Warto dodać, że w przeciwieństwie do piłki nożnej, koszykówki, rugby czy innego hokeja, esportowi kibice to w dużej mierze uczniowie szkół podstawowych, gimnazjów i liceów. Ci nie posiadają jeszcze własnego dochodu, grubego portfela ani pokaźnych zdolności nabywczych. To jeden z powodów, dla których e-sport na terenie Europy oraz Stanów Zjednoczonych wciąż jeszcze nie wszedł na salony ani tym bardziej do domowych salonów, pozostając w pokojach dzieci. To się jednak zmieni.
Slide 26
Wiele tradycyjnych sportów jest ściśle związanych z krajami pochodzenia. Polacy raczej na pewno nie rozkochają się w NFLw przeciągu kilku następnych lat, podobnie jak Amerykanie nie pokochają kopanej i Ligi Mistrzów. Sportowa mapa świata pełna jest podziałów, stref wpływów i bardzo wysokich, uwarunkowanych społecznie i kulturowo murów. Z e-sportem sytuacja wygląda inaczej. Niezależnie od konkretnej gry, jej język zawsze jest ten sam. W Counter Strike zagra Japończyk, Chińczyk, Europejczyk oraz Amerykanin. Na tabuny grających w League of Legends składają się dziesiątki ras i narodowości. Tutaj nie ma podziału na konkretne państwa i regiony. To mniej Polacy, Czesi czy Rosjanie, a bardziej gracze. Tylko gracze i aż gracze, posługujący się wspólnym kodem zwycięstw, porażek, kooperacji i rywalizacji.
Slide 27
Doskonale rozumieją to ogromne koncerny, które coraz śmielej wchodzą w obszar e-sportu, finansując zmagania graczy. Co ważne, nie są to tylko i wyłącznie podmioty związane z branżą gier i elektroniką. Pepsi, Nissan, a ostatnio również Coca-Cola będąca sponsorem ligi League of Legends wszystko to przedsiębiorstwa, które są w stanie wyłożyć bajońskie sumy, ale oczekują w zamian równie bajońskich rezultatów. To że Riot Games nie odnosi finansowych sukcesów na organizacji turniejów League of Legends wcale nie oznacza, że taki sam los czeka Coca-Colę. Wręcz przeciwnie. Spożywczy gigant doskonale rozumie, że e-sport ma globalną strukturę, nie znosi podziałów i murów, nie zajmuje się polityką ani nie wymaga infrastruktury wyrażonej w autostradach, stadionach i lotniskach. To, czego potrzebuje e-sport to kilku lat niezbędnych na wydoroślenie kibiców oraz potężnego pchnięcia, które wprowadzi rozgrywki do tradycyjnych mediów.
Slide 28
Takiego pchnięcia nie jest w stanie wykonać samo Riot Games. Tym bardziej Intel czy MSI. Tutaj potrzeba kogoś z zewnątrz, z ogromnym doświadczeniem jako mecenas, sponsor oraz fundator. Potrzeba kogoś z ogromną ilością gotówki, która nie musi zwrócić się ani w tydzień, ani w miesiąc, ani w rok, ale przynieść długofalowe, wymierne korzyści. Niezależnie, czy będzie to Pepsi, Nissan czy Coca-Cola, kto pierwszy uatrakcyjni e-sportowe rozgrywki oraz zapewni im rozgłos na miarę tradycyjnego sportu ten zgarnie całą, stale rosnącą i puchnącą w oczach pulę. To nie sponsoring. To marketing
Slide 29
Byłem pod dużym wrażeniem tego, jak wyglądały finały Intel Extreme Masters w katowickim Spodku. Jestem przekonany, że producent procesorów sporo dokłada do spektakularnej imprezy. Jak to jest? Technologiczny gigant bez mrugnięcia okiem może pozbawić pracy setki osób zamykając niewydajne projekty, ale dokłada do takiego biznesu jak e-sport? Odpowiedź jest prostsza niż może się wydawać kto do tego coraz bardziej zatłoczonego pociągu nie wsiądzie dzisiaj, jutro może już się nie zmieścić. Wiedzą o tym największe korporacje, niezależnie od oferowanych produktów. Branża żywnościowa, producenci samochodów czy podzespołów komputerowych to tak naprawdę nie ma znaczenia. Liczy się przewidywanie trendów, te z kolei są dla e-sportu bardzo obiecujące.
Slide 30
Rząd Stanów Zjednoczonych i Francja poszły na rękę wszystkim graczom, którzy parają się profesjonalną rywalizacją w międzynarodowych rozgrywkach ligowych. We Francji eSport jest oficjalnie uznawany za sport. Na mocy podjętej przez rząd Stanów Zjednoczonych decyzji, uczestniczący w ligowych rozgrywkach gracze będą traktowani w dokładnie ten sam sposób, co sportowcy z prawdziwego zdarzenia. Co to oznacza? Przede wszystkim brak konieczności ubiegania się o wizę w celu wzięcia udziału w turniejach, podczas których uczestnicy konkurują ze sobą przy komputerach i konsolach. e-sportowcy, jak nazywani są tacy gracze, będą mogli rozgrywać ligowe sesje bez zbędnych formalności, przekraczając granice USA w dokładnie ten sam sposób, co sportowcy uczestniczący w międzynarodowych zmaganiach.
Slide 31
Jestem pod wrażeniem. eSport to coraz silniej rozwijająca się gałąź rozrywki. Na jej fali sukces odniósł między innymi Twitch.tv, stanowiący dzisiaj jedno z najsilniejszych mediów streamujących materiały filmowe. Zdolność do realnego wpływu producentów gier na konstytucyjny organ władzy wykonawczej Stanów Zjednoczonych to wyjątkowe i bardzo ciekawe zjawisko. W większości przypadków to właśnie politycy wpływają na twórców i wydawców, bardzo często ograniczając ich możliwości, podnosząc raban związany z nieuzasadnioną brutalnością komputerowych produkcji czy zakazując ich dystrybucji na terenie konkretnych państw.
Slide 32
Sytuacja ulega diametralnej zmianie, o czym świadczą wyniki finansowe branży gier z ostatnich lat. W 2011 roku całkowite dochody tego segmentu rynku wyniosły więcej, niż łączne dochody z hollywoodzkiej branży filmowej, opierając się na danych z E3 oraz box office. Premiery produkcji największego kalibru, takich jak Call of Duty, pobijają kinowe otwarcia wysokobudżetowych blockbusterów. Samo Black Ops 2 w ciągu pierwszych pięciu dni zarobiło ponad miliard dolarów. W ostatnim czasie taki wynik udało się osiągnąć jedynie Avatorawi Camerona. Coraz bardziej dochowa branża gier jest dzisiaj tak samo istotnym rynkiem jak jego muzyczny czy filmowy odpowiednik. Nic więc dziwnego, że politycy coraz częściej skupiają uwagę na tej części przemysłu, idąc na rękę zarówno klientom, jak i producentom.
Slide 33
ESPORT ROŚNIE W coraz większej liczbie krajów zostaje uznawany prawnie za sport. Esportowiec to zawód przyszłości i wkrótce będzie tak samo popularny jak zawodnik piłki nożnej. Popularność niesie za sobą wzrost nakładów finansowych, które inwestują w tego typu działania sponsorzy. To jest już poważny biznes, a nie zabawa dla młodych znudzonych ludzi, którzy szukają oderwania w świecie elektronicznej rozrywki. Scena profesjonalnych graczy w Polsce rośnie i będzie rosła nadal. Wielu młodych będzie marzyło o tym aby zostać zawodowym esportowcem. Nie prawnikiem czy inżynierem.
Slide 34
Co stoi na przeszkodzie? Smutna odpowiedź brzmi: przekonania, które powodują Twój opór drogi rodzicu. To tylko głupia gra! Zniszczysz sobie wzrok i zmarnujesz życie! Nie pojedziesz na turniej, bo jesteś za młody. To nie jest przyszłość dla Ciebie. Potrzebujesz dobrej pracy na etacie.
Slide 35
Po pierwsze gry bardzo pozytywnie wpływają na koordynację, refleks, szybkość myślenia i wiele innych ważnych cech u młodzieży. Po drugie dobry monitor nie niszczy wzroku bardziej niż brak ochrony uv w słoneczny dzień. Po trzecie gdyby dziecko osiągało sukcesy w piłce nożnej a nie grach, jestem pewny, że wcale nie byłoby tak trudno znaleźć opiekuna. Po czwarte i piąte w turnieju CS:GO pula nagród sięga 1 000 000 dolarów ciekawe ile lat trzeba pracować w dobrej pracy na etacie, aby odłożyć tej sumy? Dodatkowo profesjonalni zawodnicy otrzymują stałe wynagrodzenie za swoją grę. Nie wiem ile młodych talentów zakończyło przedwcześnie karierę właśnie ze względu na opór rodziców. To jest smutne, że brak wiary w możliwości swojego dziecka potrafi zaprzepaścić realizację tak pięknych marzeń. Co musi się stać, żebyście uznali istnienie esportu w życiu waszej pociechy? Są już nawet transmisje w telewizji z turniejów i innych ważnych wydarzeń na scenie zmagań sportowców elektronicznych.
Slide 36
Oczywiście nie namawiam, aby pozwalać grać dzieciom po 12 godzin i usprawiedliwiać nieobecności w szkole. Nie tędy droga. Skuteczny i poprawnie stworzony trening nie zajmie więcej niż 2 - 4 godziny dziennie, a zagwarantuje stałe podnoszenie umiejętności. Podczas mojej pracy z młodymi zawodnikami stworzyłem już setki takich programów treningowych. Dodatkowo moi podopieczni zawsze są uczulani na to, że do rozwoju nie wystarczy tylko granie. Mocno naciskam na to, aby wprowadzili do swojego życia regularny wysiłek fizyczny, spotkania ze znajomymi, a nawet odpowiednią dietę. Podchodzę do rozwoju młodego zawodnika holistycznie, dzięki czemu stwarzam odpowiednie warunki do tego, aby taki gracz mógł w przyszłości być prawdziwym zawodowcem. Wystarczy mądre podejście do tematu i wspieranie na drodze rozwoju, a wszystko staje się możliwe.
Slide 37
Warto też rozgraniczyć pojęcia granie a trening. Granie z reguły polega na zabawie i relaksowaniu się podczas grania. Trening jest dużo mniej przyjemny jednak pozwala na kontrolowany rozwój umiejętności. Jeżeli widzisz drogi rodzicu, że twoje dziecko ma regularne treningi z zespołem, czyta, rozwija się i często siedzi samo na serwerze wykonując nudne czynności to właśnie rośnie Ci młody sportowiec elektroniczny. Wspieraj, wspieraj i jeszcze raz wspieraj. Zapytaj o to, co robi, zainteresuj się. Zawieź na turniej, pomóż w opłacie noclegu w innym mieście. Zrozum, że to jest TO, co twoja pociecha chce robić w życiu i pomagaj. A najważniejsze zaakceptuj wybór, jakiego dokonała ta młoda osoba. W końcu kiedyś musi nauczyć się dokonywania wyborów, dyscypliny i samodzielności, prawda?
Slide 38
Na świecie jest 256 mln miłośników e-sportu. Ich charakterystyka znacząco odbiega od stereotypu są w średnim wieku, dobrze zarabiają i mają stałą pracę. Co ciekawe 40 w ogóle nie gra, lecz tylko kibicuje. E-sport to jedna z najdynamiczniej rozwijających się gałęzi rozrywki. Szacuje się, że wartość rynku e-sportowego w 2016 roku wyniesie 465 mln dolarów, aby w roku 2019 osiągnąć 1,1 mld dolarów. Także w Polsce e-sport znajduje się na fali wzrostowej. Szacuje się, że w 2016 roku wartość rynku e-sportowego w naszym kraju wyniesie 40 mln złotych, a za 2 lata, w 2018 roku sięgnie 52 mln złotych. E-sport to jednak nie tylko zawodnicy, rozgrywki i wielkie pieniądze to przede wszystkim fani. Kim są?
Slide 39
1. Liczba miłośników e-sportu w latach 2016-2019 wzrośnie z obecnych 256 do 345 mln. 2. Spośród 256 mln fanów e-sportu, 131 mln stanowią wierni entuzjaści, a 125 mln widzowie okazjonalni, którzy oglądają głównie najważniejsze imprezy. 3. 40 miłośników e-sportu jedynie kibicuje. Sami nie grają. Zdziwieni? Pomyślcie ilu kibiców piłki nożnej aktywnie gra w piłkę, a ilu faktycznie uprawia ten sport. W esporcie jest podobnie. 4. Najwięcej fanów e-sportu znajduje się w Azji i Oceanii (44). Nasz kontynent Europa to druga siła na świecie. Pochodzi z niej aż 25 oglądających e-sport. 19 fanów znajduje się w Ameryce Północnej, a pozostałe 12 ulokowanych jest w innych częściach naszego globu. 5. Polska jest najważniejszym rynkiem e-sportowym wśród krajów Europy Wschodniej. Jak wypadamy na tle Europy Zachodniej?
Slide 40
6. Aż 73 miłośników e-sportu ma powyżej 21 lat. Tylko 27 zalicza się do przedziału wiekowego 10-20 lat. To przeczy stereotypowemu wizerunkowi młodego widza. 7. Fani e-sportu to sami panowie. Jesteście w błędzie! Faktycznie mężczyźni stanowią 68 e-sportowej publiki, natomiast liczba fanek e-sportu rośnie w siłę i aktualnie wynosi już 32. 8. Czy przeciętny miłośnik e-sportu pracuje? Owszem i co dla wielu osób będzie zaskoczeniem aż 63 reprezentantów tej grupy ma stałą pracę. Wśród typowych użytkowników Internetu tylko 48 ma stałe zatrudnienie. 9. Fan e-sportu, a zarobki. E-sportowa publika to dobrze zarabiająca publika. Wynika to pośrednio z większego odsetka osób dysponujących stałą pracą, o czym wspomnieliśmy w fakcie 8. Statystyki pokazują, że 48 fanów e-sportu zaliczyć można do grupy dobrze zarabiających. Tylko 34 spośród typowych użytkowników Internetu może pochwalić się przynależnością do tej kategorii. 10. Entuzjasta e-sportu wydaje więcej na sprzęt. 21,1 entuzjastów e-sportu przeznacza na zakupy sprzętu ponad 600 dolarów rocznie. Tylko 9,7 ogółu graczy przeznacza na sprzęt taką kwotę. Jak widać fan e-sportu to także dobry klient branży IT.
Slide 41
Pomimo niższej o 62 liczby Internautów (27,2 mln w Europie Wschodniej vs 71,2 mln w Europie Zachodniej) liczba widzów e-sportu w naszym regionie w 2019 roku ma być tylko o 15 niższa niż w Europie Zachodniej. Pomimo znacznie niższej liczby graczy 13,7 mln w Europie Wschodniej i 41 mln w Europie Zachodniej przewiduje się, że w 2019 roku liczba widzów e-sportu podzielonych na regularnych i okazjonalnych wyniesie w Europie Wschodniej 14 i 20 mln, natomiast w Europie Zachodniej odpowiednio 22 i 23 mln. Biorąc pod uwagę liczebność społeczeństwa i liczbę graczy różnice będą niewielkie. Aktualnie, w 2016 roku liczba widzów e-sportu w Europie Wschodniej wyniesie 10mln (regularni) i 15 mln (okazjonalni).
Slide 42
Czytając powyższe dane nie powinniście mieć wątpliwości, dlaczego esport ciągle nabiera na sile. Nawet w Polsce mamy już szkołę, gdzie jest utworzona klasa poświęcona elektronicznym rozgrywkom. Nie brakuje u nas wydarzeń typu Intel Extreme Masters, PGA czy WGW. Co roku setki tysięcy fanów w naszym kraju mogą na żywo oglądać zmagania najlepszych drużyn na świecie. Można dalej uważać, że gry są dla dzieci, że są głupie, tylko, kto będzie w stanie to dobrze uargumentować, jeżeli mamy naprawdę mocne dowody na podważenie tej tezy? Nic nie wskazuje na to, że za kilka lat coś może pójść nie tak. Ludzie uwielbiają oglądać mecze w CS:GO, LoL, DOTA 2, WoT i wielu innych gier. Chcą wspierać swoich idoli, a także samemu próbować swoich sił w wymienionych produkcjach. Cieszę się, że od pewnego czasu wszystko to, co związane z esportem zmienia się na lepsze i większe. Nie brakuje rzeczy, które wypadałoby poprawić, usprawnić, albo w ogóle dodać do tego zjawiska, ale wierzę, że na wszystko przyjdzie czas.
Slide 43
Profile czy szkoły e-sportowe nie są niczym nadzwyczajnym szczególnie w Azji. W Polsce jednak nic takiego nie miało dotychczas miejsca. Wygląda na to, że technikum w Kędzierzynie-Koźlu przetrze szlaki. Uczniowie Kędzierzyńsko Kozielskiego ZSTiO obok uczenia się tego, jak tworzyć gry, będą trenować i reprezentować szkołę w rozgrywkach Counter-Strike: Global Offensive. Rozwieję jednak od razu wątpliwości (i nadzieje) wszystkich osób, które myślą, że będą chodzić [] Profile czy szkoły e-sportowe nie są niczym nadzwyczajnym szczególnie w Azji. W Polsce jednak nic takiego nie miało dotychczas miejsca. Wygląda na to, że technikum w Kędzierzynie-Koźlu przetrze szlaki. Uczniowie Kędzierzyńsko Kozielskiego ZSTiO obok uczenia się tego, jak tworzyć gry, będą trenować i reprezentować szkołę w rozgrywkach Counter-Strike: Global Offensive.
Slide 44
Rozwieję jednak od razu wątpliwości (i nadzieje) wszystkich osób, które myślą, że będą chodzić do technikum i od rana do popołudnia grać w gry, nie robiąc niczego innego. Nic z tych rzeczy. Klasa e-sportowa nie będzie klasą o profilu e-sportowym w dosłownym tego słowa znaczeniu. Będzie to klasa informatyczna o profilu tworzenie gier i e-sport. Uczniowie będą uczyć się w niej między innymi matematyki, grafiki, programowania itp. Poznają możliwości tworzenia gier, silnika source i pracy w Workshop. Na zajęciach poruszane będą również tematy silników gier (Unreal Engine, Unity 3D). Każdy absolwent otrzyma tytuł technika informatyka. Oczywiście nie ominie ich też klasyczna matura.
Slide 45
No dobrze, to kiedy uczniowie będą grać? Niestety nie w godzinach lekcyjnych. Klasa ma posiadać trzy 5-osobowe drużyny e-sportowe: turniejową dwie drużyny rezerwy. Nabór oraz roszady w drużynach będą przeprowadzane na bieżąco przy uwzględnieniu aktualnej dyspozycji uczniów. W przypadku braku rokujących zawodników możliwe jest wyłonienie drużyn z całego kierunku przy uwzględnieniu klas starszych. Treningi oraz zajęcia teoretyczne e-sportowe odbędą się w ramach godzin dodatkowych. Zakładamy, że podczas naboru uda się stworzyć 30-osobową klasę, w której znajdzie się co najmniej 15 osób, które będą mogły stworzyć perspektywiczną i zgraną drużynę esportową.
Slide 46
Co jednak ciekawe, szkoła zapewni potrzebny do treningów sprzęt, sfinansuje wyjazdy na turnieje i noclegi, a także zapewni opiekę psychologa dla drużyny. Technikum liczy na nawiązanie współpracy z organizacjami e-sportowymi, by zawodnicy mogli trenować z najlepszymi. Chęć współpracy zgłosiły już niemieckie myRevenge oraz Polska Black Ravens, wszystko jest więc na dobrej drodze
Slide 47
PROFESJONALNE LIGI E-Sports Entertainment League (międzynarodowa) UKeSA Dell XPS Premiership (brytyjska) Cyber Evolution (międzynarodowa) National Professional Cybersport League (rosyjska) ESL Extreme Masters (międzynarodowa) Athens Gaming League (grecka) Electronic Sports World Cup (międzynarodowa) Global Gaming League (koreańskamiędzynarodowa) World Cyber Games (międzynarodowa) DreamHack (europejska) Poznań Game Arena (europejska) masterleague.eu (europejska) World e-Sports Games (międzynarodowa) Liga Cybersport (polska) ESL Major Series (europejska) The League of Legends Championship Series (LCS) (europejska) ESL Pro Series (w poszczególnych krajach Europy) NGL One (europejska) The League of Legends Championship Series (NA LCS) (północnoamerykańska) ClanBase EuroCup (europejska) League of Legends Champions Korea (LCK) (koreańska) Total Gaming League (międzynarodowa) The Tencent League of Legends Pro League (LPL) (chińska) Pro Gaming League (północnoamerykańska)
Slide 48
Stowarzyszenia i organy rządowe International eSport Federation (międzynarodowa) eSport Verband Österreich (Austria) Belgian Electronic Sport Federation (Belgia) E-Sport Denmark (Dania) Deutscher eSport Bund (Niemcy) Nederlandse Electronic Sport Bond (Holandia) Swiss E-sport Federation (Szwajcaria) Korea e-Sports Association (Korea Południowa) Taiwan eSports League (Republika Chińska) United Kingdom eSports Association (Wielka Brytania) eSports Vietnam (Wietnam) Mind Sports South Africa
Slide 49
Film
Dane:
- Liczba slajdów: 49
- Rozmiar: 5.55 MB
- Ilość pobrań: 1368
- Ilość wyświetleń: 19022